A Agência Nacional de Vigilância Sanitária (ANVISA) declara que seus processos de regulamentação seguem os mais altos graus de transparência e qualidade técnica, mas quando analisamos algumas decisões tomadas pela agência ao longo da discussão sobre a regulamentação dos cigarros eletrônicos no Brasil, isso não fica muito claro.
No momento, há uma consulta pública em curso que está perguntando para a sociedade o que ela pensa sobre um novo texto proposto ao tema, que substituiria a atual legislação sobre os cigarros eletrônicos no Brasil, definida pela RDC 46 de 2009 que proíbe o comércio, importação e propaganda dos produtos.
O novo texto mantém a proibição e endurece ainda mais as regras, proibindo também a fabricação e até usando as palavras “transporte” e “armazenamento”, sem definir o que quer dizer com isso.
O DIRETA – Diretório de Informações para Redução dos Danos do Tabagismo, uma organização não governamental, sem fins lucrativos, que representa milhares de consumidores brasileiros de cigarros eletrônicos, enviou um comunicado para a Anvisa questionando esses pontos em 05 de Dezembro de 2023 e até o momento não recebeu retorno.
Alexandro Lucian, presidente do DIRETA disse: “Encaminhamos ofício questionando exatamente o uso das palavras “transporte” e “armazenamento” no novo texto proposto pela Anvisa para regulamentar os cigarros eletrônicos. São palavras muito abrangentes que não são explicadas no texto, ao contrário de outros termos como “produto fumígeno” ou “dispositivos eletrônicos para fumar”, cuja definição é expressada em detalhes.”
Sem uma resposta, o Brasil não sabe o que a Anvisa quer dizer com isso. Será proibido para um consumidor “transportar” seu produto no bolso ou na mochila enquanto vai para o trabalho? E guardar na gaveta ou no armário de casa entra na definição de “armazenamento”?
“Em consulta com vários especialistas jurídicos, o consenso é de que o texto atual vai acabar criminalizando milhões de consumidores de cigarros eletrônicos no Brasil, proibindo na prática a posse e o uso dos produtos, o que nunca ocorreu até hoje.” complementa Alexandro Lucian.
Além do texto que traz muitas dúvidas, o processo de consulta pública em si também apresenta uma dificuldade desnecessária em vários pontos.
O acesso é feito através do site da Anvisa, que com frequência fica fora do ar ou não carrega corretamente.
Após passar pela verificação de segurança, o interessado em participar é recebido com um grande texto contendo informações diversas. Em uma delas é dito que “Em caso de dúvidas relacionadas ao assunto da proposta de norma encaminhe e-mail para def@anvisa.gov.br“. Em 12 de Dezembro de 2023 foi enviada uma comunicação para o endereço de email informado e recebida uma resposta automática sem qualquer relevância com o assunto:

Dificuldades para quem não fala português
Ao se identificar, além do nome completo e endereço de email, é preciso responder se a contribuição é national ou internacional.
Este é um ponto importante. No Brasil há uma total falta de conteúdo científico sobre cigarros eletrônicos porque até para este fim as importações são proibidas. É possível pesquisar em laboratório sobre cocaína, mas não sobre cigarro eletrônico. Por causa disso, muitas contribuições serão realizadas por especialistas internacionais do controle do tabaco e para isso a consulta pública não traz nenhuma facilidade.
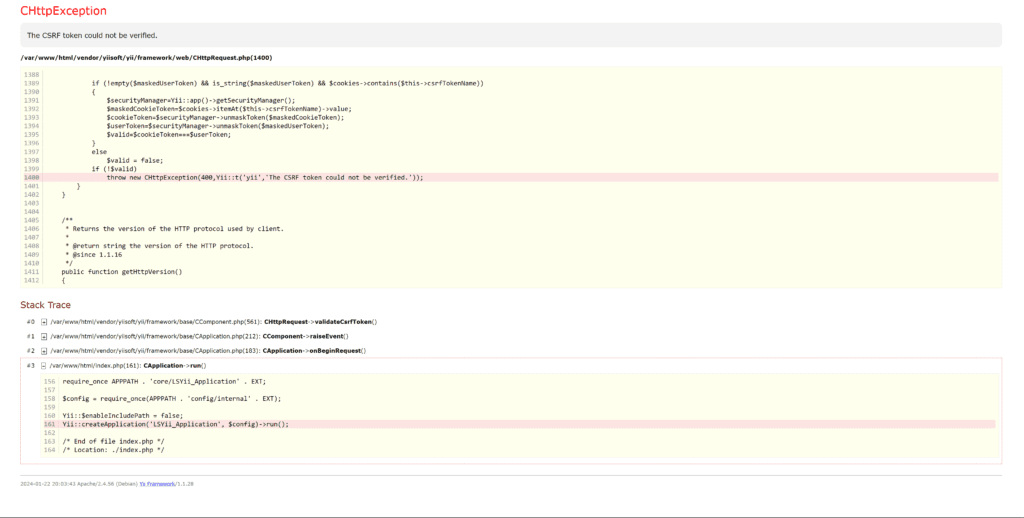
Mesmo optando por “internacional”, não há tradução para a língua inglesa. Quem tentar utilizar o Google tradutor para acessar o site já traduzido, receberá um erro de código que impede a participação:
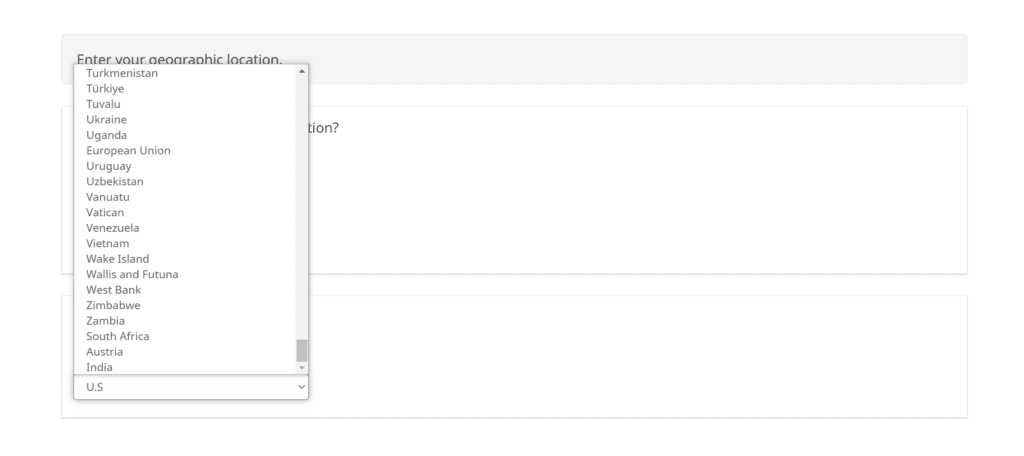
Caso use o próprio navegador para isso, ferramenta presente no Google Chrome por exemplo, vai enfrentar outras dificuldades, como a lista de países que perde totalmente sua ordem alfabética, tornando complicado achar a opção para os Estados Unidos, que na caixa de seleção se transforma em U.S., além da Áustria e a Índia ficarem em último lugar para escolha, misturadas com países que começam com a letra W e Z.
Contribuições populares podem ser ignoradas
Após se identificar, é preciso dizer como você gostaria de contribuir com a consulta pública: deixar uma opinião ou contribuir individualmente nos artigos da proposta. Em seguida, é feita a pergunta “Você é a favor desta proposta de norma?” com as respostas “sim” ou “tenho outra opinião”. Qualquer pessoa que não concorde irá optar pela segunda opção, onde um novo campo é oferecido para justificativa.

A opção de deixar opiniões sobre a proposta será a mais utilizada pela população em geral, especialmente consumidores. Nela consta o seguinte texto:
“Atenção:
Este espaço serve para o participante comentar, do ponto de vista particular, a proposta normativa que está em consulta pública. Por se tratar de comentários de cunho pessoal, sem argumentação ou evidências, não exige um posicionamento da Agência, em contrapartida oportuna o conhecimento do problema pela área técnica responsável.”
Da forma como é escrito, parece que a contribuição popular não terá qualquer relevância, uma vez que a Anvisa já alerta que não se comprometerá a dar um posicionamento, o que pode incentivar muitas pessoas a simplesmente desistir de participar.

Trabalhos acadêmicos não serão considerados
Ao final da consulta há uma opção para envio de arquivo, cujo texto não deixa claro para que serve, uma vez que diz “Atenção: Este campo NÃO deve ser utilizado para inserir contribuições acerca dos dispositivos da proposta normativa, pois nesse caso, as contribuições nele contidas NÃO serão analisadas. Utilize o campo específico para isso.“

Se ele não pode ser usado para enviar contribuições, para que então ele existe?
Muitas organizações internacionais e especialistas independentes já produziram material específico para a discussão da regulamentação dos cigarros eletrônicos no Brasil, preocupados com as decisões proibitivas que alimentam um cenário de mercado ilegal e consumo indiscriminado, com riscos à saúde, acesso aos jovens e muitos outros problemas, indo na contramão de mais de 100 países que já permitem um comércio controlado dos produtos. Há trabalhos de profissionais renomados, como relatórios, estudos e críticas, apresentados em documentos que poderiam ser anexados na consulta, mas que a Anvisa impede que sejam levados em consideração de uma forma arbitrária, o que dificulta o recebimento de conteúdo relevante para a saúde pública brasileira.
Última pergunta não é clara e induz ao erro
A última pergunta da consulta pública apresenta um formato que está levando muitas pessoas ao erro. Nela temos: “Você considera que a proposta de norma possui impactos:” cujas escolhas são “positivos”, “negativos” e “positivos e negativos”.
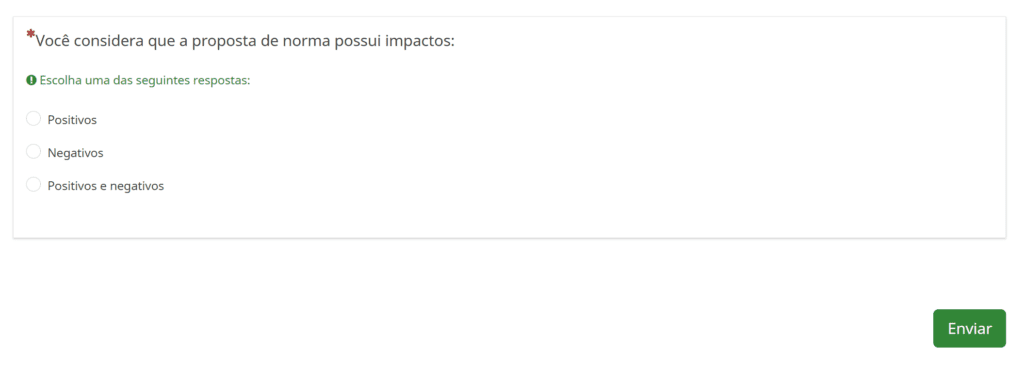
Nas mídias sociais e em grupos de Whatsapp temos visto pessoas que não concordam com o texto, mas que estão escolhendo a opção “positivos”, porque interpretam que a pergunta está se referindo ao ato de se ter regras, controle e normas sobre o assunto de uma maneira geral, o que consideram que não existem no momento, dado o grande comércio ilegal e consumo indiscriminado no país.
Neste sentido, quem defende a permissão do comércio de cigarros eletrônicos no Brasil, também defende a criação de propostas de norma, pois isso claramente trará impactos positivos.
O que a pergunta realmente quer saber é se você concorda ou não com as normas específicas estabelecidas no novo texto, que são direcionadas a um ambiente proibitivo. Quem não concorda com o texto, consequentemente acredita que ele traz consequências negativas, porém várias pessoas estão divulgando nas mídias sociais que precisaram refazer sua participação na consulta pública e corrigir sua participação, pois responderam “positivos” e justificaram com críticas à proibição, defendendo a criação de normas para a venda controlada dos produtos. Neste caso, a verdadeira intenção dessas pessoas era a opção “negativos”, alinhada com a justificativa que apresentaram.
Dúvidas em relação ao processo
É preciso lembrar que o texto proposta na atual consulta pública, que mantém a proibição do comércio de cigarros eletrônicos e endurece ainda mais as regras, foi baseado em um relatório criado por uma área interna da Anvisa e entregue em Abril de 2022 após vários atrasos, chamado de Relatório de Análise de Impacto Regulatório (AIR).
Antes da aprovação deste relatório, em 10 de Junho de 2022, a Anvisa cumpriu a TPS – Tomada Pública de Subsídios, etapa em que mais uma vez convidou a sociedade e partes interessadas a contribuir com o tema, enviando comentários sobre o relatório, na época em sua fase parcial, além de novos documentos para análise, o que serviria para ajudar a compor a versão final do AIR.
Ao pesquisar quem foi que contribuiu nesse processo, descobrimos que o DIRETA enviou um documento de 78 páginas com uma crítica detalhada ao AIR no dia 09 de Junho, um dia antes do prazo final da TPS. Também confirmamos informações de especialistas e profissionais independentes do controle do tabaco que contribuíram nos últimos dias de prazo da TPS enviando grande grande quantidade de material.
Confirmamos ainda que houve considerável contribuição da indústria tabagista, que também oficializou sua participação em data próxima do prazo final da TPS, com centenas de páginas de documentos técnicos e científicos.
Apesar de tudo isso, passados apenas 2 dias úteis do final desse prazo, no dia 14 de Junho, foi marcada reunião ordinária para o dia 22 do mesmo mês, cujas pautas incluíam a análise do Relatório AIR e a deliberação sobre uma nova consulta pública, cuja relatora era a Dra. Cristiane Jourdan.
Essa reunião foi marcada fora da sequência tradicional de um processo regulatório da agência e mostrou uma pressa desproporcional da Dra. Cristiane Jourdan sobre o tema. Do final do prazo da TPS no dia 10 de Junho até a data da reunião foram passados somente 12 dias corridos, que deveriam ser suficientes para analisar milhares de páginas de documentos.
Um detalhe importante a considerar é que a Dra. Cristiane Jourdan estava com data de saída da Anvisa garantida, marcada para 24 de Julho do mesmo ano, apesar de suas tentativas judiciais de se manter na agência, todas indeferidas. Resta saber o porquê um tema tão relevante e importante para a saúde pública brasileira foi tratado com tanta pressa, ficando sob responsabilidade de alguém prestes a deixar o cargo, que brigava na justiça para continuar na agência e que parecia querer resolvê-lo desobedecendo um processo normal, que deveria se estender além do mandato da funcionária.
O clima parecia tão tenso que, em reunião extraordinária no dia 21/06/2022, um dia antes da reunião marcada para discutir sobre os cigarros eletrônicos, ao deliberar sobre uma ação judicial que exigia a suspensão do agrotóxico Carbendazim, suspeito de provocar câncer, prejudicar a capacidade reprodutiva humana e afetar o desenvolvimento, a relatora Dra. Cristiane Jourdan discutiu com sua colega, a diretora-substituta Meiruze Freitas e abandonou a chamada ao vivo, causando grande desconforto aos outros diretores, que por conta disso decidiram cancelar a reunião do dia seguinte.
Mas a diretora Dra. Cristiane Jourdan rapidamente marcou nova reunião para tratar do relatório AIR em 29/06, desta vez extraordinária e exclusiva para o assunto, marcada para acontecer no dia 06/07, apesar de já existir uma reunião ordinária no mesmo dia, o que é bastante incomum.
A reunião ocorreu conforme agenda e após um longo voto que durou horas, Dra. Cristiane Jourdan aprovou o relatório AIR e os diretores seguiram com ela. Hoje, a consulta pública trata de um texto que foi totalmente baseado nesse relatório, aprovado às pressas em um processo que traz dúvidas na forma como ele foi conduzido.